Hvis man skal arbejde nærmere med kiralitet, er det godt at kende lidt til navngivningen af molekylerne og også at forstå nogle forhold ved den almindelige omtale af disse molekyler.
Denne side forsøger at give et overblik. Mange specialformer er ikke nævnt her, men der er henvisning til mere information nederst på siden.
Kirale molekylers historie
Louis Pasteur noteres normalt for opdagelsen af kirale molekyler, og det er da også rigtigt at Pasteur har bidraget til opdagelsen, men som han selv gør opmærksom på i sin præsentation fra 1860 (Pasteur 1861) så skulle det polariserede lys lige opdages først i begyndelsen af 1800-tallet og dernæst var det den franske forsker Biot der i 1815 først beskrev det fænomen at organiske molekyler, der var opløst i vand kunne bøje polariseret lys til højre eller venstre – lige som det allerede var kendt at visse faste krystaller kunne. Det var altså andre forskere der opdagede det kirale fænomen, men Pasteur arbejdede systematisk med fænomenet, og præsenterede det for en større kreds af forskere (Pasteur 1848 og 1861)
Omtale af kirale molekyler
Kiral: Bruges om molekyler som indholder et eller flere kirale centre, hvilket igen normalt forudsætter at der er et atom som kan binde sig til fire forskellige atomer eller molekyler. Det mest almindelige er kulstof C, men enkelte stoffer har et kiralt fosfor P, kvælstof N og svovl S. Gerannium Ge og Silikat Si kan også danne kirale forbindelser, men indgår indtil videre sjældent i organiske forbindelser. Den engelske betegnelse er “chirale”.
Enantiomer: Er betegnelsen for et par af kirale molekyler der er nøjagtige spejlbilleder at hinanden. Enantiomere molekyler har nøjagtig samme fysiske egenskaber, som f.eks frysepunkt og kogepunkt, men har forskellige bio-kemiske reaktioner, når det kommer i forbindelse med levende celler eller andre kirale overflader eller processer og har derfor normalt forskellige fysiologiske effekter på mikroorganismer, svampe, planter og dyr. Derfor har de også normalt forskellig giftighed og de nedbrydes med forskellig hastighed. E-vitamin betegnes RRR-alfa-tochopherol og dets enantimoere form er SSS-alfa-tochopherol. Den engelske betegnelse er “enantiomers”.
Racemat / Racemisk: Betegner en blanding af enantiomerer, når de findes i en opløsning i lige store mængder altså 1:1. En racemisk blanding vil ikke afbøje lys. Den normale forkortelse for et racemat er rac., LD eller RS, f.eks. Alfa-tocopherol (rac.) eller LD-Alfa-tocopherol. Den engelske betegnelse er “racemic”.
Diasteromer: anvendes til at betegne par af et kiralt molekyl,e som har 2 eller flere kirale centre, men som ikke er et enantiomert par. Som eksempel betegnes E vitamin kemisk set som RRR-alfa-tochopherol som danner et enantiomert par med SSS-alfa-tochopherol, mens de former der betegnes RRS, RSR, RSS, SRR, SRS og SSR alle er diastomere i forhold til RRR-alfa-tocophe rol. Diastomere par har hverken samme fysiske eller bio-kemiske karakteristika, og det betyder at de f.eks. normalt vil have forskelligt frysepunkt og kogepunkt ud over at de også vil reagere forskelligt i levende organismer.
rol. Diastomere par har hverken samme fysiske eller bio-kemiske karakteristika, og det betyder at de f.eks. normalt vil have forskelligt frysepunkt og kogepunkt ud over at de også vil reagere forskelligt i levende organismer.
Illustrationen viser ephedrins enantiomere og diastomere former. Ephedrin har 2 kirale centre, og hver af de 4 kirale former er derfor hver især del af et enantiomert par og der er derfor også 2 diastomere former.
Enantiopure: Betegner et stof hvor kun den ene enantiomer af et stof forekommer.
Homochiral: er det faglige begreb for, at livet normalt kun anvender den ene type af enantiomere par, som det er kendt at livet kun anvender L-aminosyrer og D-sukkerstoffer (Ozturk 2023).
Unichiral: Har i princippet samme betydning som Enantiopure, men undgår at bruge begrebet “enantio” som jo er knyttet til par af molekyler.
Navngivning af kirale molekyler
(+) og (-) . Den oprindelige navngivning af kirale molekyler skyldes at Louis Pasteur opdagede at vinsyre fandtes i to former – en form som drejede ultraviolet polariseret lys til højre (+) og en anden form der kastede lyset til venstre (-). Denne navngivning anvendes jævnligt i dag, men står aldrig alene i moderne litteratur om kirale molekyler
Problemet med denne navngivning er, at man ikke ud fra et molekyles sammensætning af atomer kan vide hvilken vej det vil kaste lyset. Derfor kan man ikke navngive molekylet før man har oprenset nok af det til at man kan kaste lys igennem, for at se hvilken en af enantiomererne der skal kaldes for (+) og hvilken for (-).
En anden grund til at man har forladt denne navngivning er, at mange kirale molekyler indeholder flere kirale centre, således at den optiske måling bliver mindre tydelig eller umulig at tolke.
L og D Navngivning med L og D (samme som l og d) bygger videre på (+)(-) navngivning som anvendte polariseret lys. I L og D navngivningen har man taget et konkret stof: Glyceraldehyd, hvor (-) og (+) formerne var kendte og man kaldte derefter den venstredrejende for L-glyceraldehyd, og den højredrejende for D-glyceraldehyd (L står vor levo som betyder venstre og D står for dextro som betyder højre). Når man skal regne ud om et konkret kiralt molekyle er L eller D, må man ifølge visse regler afklare om det nye molekyle ligner L eller D Glyceraldehyd mest – eller hvilken form det lettest kan udbygges til at ligne.
Man betegner så stoffet L eller D – uanset om det nye stof faktisk drejer lyset samme vej som L eller D Glyceraldehyd. Denne navngivning bliver fortsat brugt meget almindeligt for de kirale stoffer som vi kender allerbedst som f.eks. de forskellige aminosyrer og sukkerstoffer som f.eks. L-lysin eller D-fructose.
Problemet med denne navngivning er, at det er meget vanskeligt – eller umuligt – at anvende de regler der gælder for L og D navngivningen til mere komplekse molekyler.
R og S Navngivning med R og S er den navngivning der anvendes i dag. Den anvendes helt normalt til nye og større molekyler og til molekyler som har flere kirale centre. Med R og S navngivningen er det forholdsvis enkelt at navngive hvert enkelt kiralt center med et R eller et S. Man kan således f.eks. se et kiralt molekyle omtalt som RRR alfa-tokoferol (naturligt E vitamin) eller SSR alfa-tokoferol-acetat (som er et kemisk fremstillet molekyle der ligner E-vitamin meget, men som ikke har nogen væsentlig E-vitamin virkning.
Nedenstående figur viser reglen for RS-navngivning.
 Det kirale centrum lægges i centrum af hånden. Hver af de 4 bindinger til centret gives et nummer 1-4 ud fra atomvægten af de 4 atomer der danner bindingen. Det letteste molekyle benævnes nr. 4 og vendes bort – altså ned mellem fingrene i hånden(i eksemplet til venstre H-atomet) så de tre andre atomer (eller molekyler) ligger i håndfladen. De tre kan nu tælles i en rækkefølge efter vægt: 1, 2 og 3 der enten går med uret og altså være R (Rectus) eller mod uret og altså være S (Sinistre).
Det kirale centrum lægges i centrum af hånden. Hver af de 4 bindinger til centret gives et nummer 1-4 ud fra atomvægten af de 4 atomer der danner bindingen. Det letteste molekyle benævnes nr. 4 og vendes bort – altså ned mellem fingrene i hånden(i eksemplet til venstre H-atomet) så de tre andre atomer (eller molekyler) ligger i håndfladen. De tre kan nu tælles i en rækkefølge efter vægt: 1, 2 og 3 der enten går med uret og altså være R (Rectus) eller mod uret og altså være S (Sinistre).
I eksemplet ovenfor er kvælstof N det tungeste og altså nr. 1 – men både 2 og 3 er kulstof atomer C, så herudfra kan man ikke afgøre hvilket der er tungest af de to og derfor nummer 2, og man går derfor videre til det næste atom hvor man finder ilt O som er tungere end brint H og derfor bliver COOH nr 2 og CH3 nr 3. Når man så skal tælle 1, 2 og 3 så må man enten gå med uret eller mod uret. Med uret betegnes så med et R og mod uret med et S. Se nærmere f.eks under reference KU.
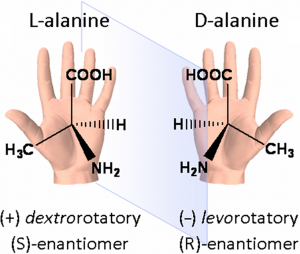
Ovenstående illustration viser også at de tre former for navngivning ikke er sammenhængende. Selv om et stof er (+) kan man ikke gå ud fra, at det så også er D og R, og hvis man ved at stoffet er L, kan man ikke vide om det så også er (-) og S. Illustrationen viser det mix som de forskellige navngivningsregler giver for alanin.
Referencer og til videre læsning:
- Enantiomers & Diastereomers
- Enantiomers
- KU om chiralitet
- Moss A.P. (1996) (IUPAC) Basic terminology of stereochemistry
- Pasteur L (1861) First Lecture from Leçons de chimie professées en 1860 (engelsk oversættelse)
- Pasteur L. (1948) Recherches sur les relations qui peuvent exister entre la forme cristalline, la composition chimique et les sens de la polarisation rotatoire. Annales Chimie Phys 24. pp. 442-459.
- Om R S momenklatur
- Om Kiralt kvælstof N Nitrogen inversion
- Om kiralt svovl S (meget nørdet)
Spørgsmål og ris og ros kan sendes nederst på forsiden.
Denne side er skrevet af og vedligeholdes af Klaus Sall, Sall&Sall Rådgivning, Brabrand. CVR: 36119756. Tlf.: 20722 6220.
Jeg har vist lige set lyset (tak for det)
Betyder det så at stofferne
“(-)-Limonene” er det samme som “D-limonene” og
“(+)-Limonene” er det samme som “L-limonene”
På forhånd tak
Njaaa . . .
– som du ved så er (+) og (-) rene optiske bestemmelser på grundlag af forsøg med polariseret lys gennem unikiralt stof
– L og D er bestemt ud fra molekyleopbygningen hos glyceraldehyd som man kender (+) og (-) formen af, og som man så sammenligner ethvert andet stof med. Det der mest ligner L henholdsvis D betegner man så uden nogen måling som L eller D.
Der er derfor ikke nogen streng logisk sammenhæng mellem (+) og Dextro eller (-) og Levo.
Hvis du vil kende den autoriserede sammenhæng for et stof er du derfor nødt til at søge på “stoffets navn” L D (+) (-) – så kommer der som regel noget fornuftigt frem
Det har jeg så gjort og fandt f.eks. den her side hvor forskellige navne for det samme stof er angivet:
https://pubchem.ncbi.nlm.nih.gov/compound/___-Limonene
Heraf fremgår det at (D)-(+)-Limonene og heraf følger (L)-(−)-Limonene.
Det fremgår også at R også svarer til (+) enantiomeren.
Mange hilsner
Klaus
Tak for hurtigt svar
Men pokkers da også.
Så (+)-limonene er altså det samme som (-)-limonene
så selvom det er forskellige former betragtes det som der samme stof ?
På PubChem siden angives der også 2 forskellige CAS-numre for stoffet
5989-27-5 og 65996-98-7
Vid det sige, at der ikke findes nogen “sandhed” ved navngivning af kemiske stoffer ?
Undskyld hvis jeg ikke skriver det helt klart. Hermed uden bindestreger – som let forveksles med minus (-):
D Limonene = (+) Limonene og heraf følger L Limonene = (−) Limonene.
Mange hilsner
Klaus
Undskyld men…
På PubChems side om D-Limonene angives som MeSH Synonyms både “(+)-limonene” og “(-)-limonene”.
Vil det sige, at der ikke findes nogen “sandhed” ved navngivning af kemiske stoffer og deres “kiralitet”?
På Pub chems hjemmeside på dette link: https://pubchem.ncbi.nlm.nih.gov/compound/___-Limonene#section=Top
øverst på siden er der en linje der hedder Chemical names. Den siger sådan her
Chemical Names: D-Limonene; (+)-Limonene; 5989-27-5; (R)-(+)-Limonene; (+)-(4R)-Limonene; (+)-carvene
Sidst i denne linje er der et felt der hedder [more] hvis du trykker på det kommer du til punkt 3.4.2. på samme side som giver 30 synonymer. Ingen af dem er (-) Limonene.
Jeg tror derfor at du kan regne med at der findes en fuldstændig troværdig og entydig navngivning for kirale molekyler.
Mange hilsner
Klaus
På siden https://pubchem.ncbi.nlm.nih.gov/compound/___-Limonene#section=Top
trykker jeg “more” ved navnene, så den hopper til 3.4 Synonymer
Under 3.4.1 MeSH synonyms (19.stk) står som nr 2 og 3 “(+)-limonene” og “(-)-limonene”
De står ikke begge 2 i 3.4.2 “Depositor-Supplied Synonyms” (130 stk.), men de er jo “provided by individual data contributors”
Venlig hilsen
Erik
Hvis vi går tilbage til dit oprindelige spørgsmål, så var det om: “(-)-Limonene” er det samme som “D-limonene” etc. De steder jeg har kunnet finde hvor både (+) OG L eller D navgivningen er angivet er det konsekvent sådan at (+) henholdsvis (-) er kombineret således: D (+)-Limonene og L (-) Limonene se f.eks. her https://monographs.iarc.fr/ENG/Monographs/vol73/mono73-16.pdf
Jeg mener derfor fortsat at du roligt kan gå ud fra at der er en entydig og retvisende navngivning for kirale molekyler.
Mange hilsner
Klaus
Men, der er altså ikke een facitliste, som angiver svaret på om hvilke stoffer der er identiske.
Tak for din store indsats for at forklare mig hvordan tingene hænger sammen.
Erik
Korrekt. Man er nødt til at afklare det i hvert enkelt tilfælde.
Mange hilsner
Klaus